行業資訊
2018年飛(fēi)檢大(dà)幕拉開

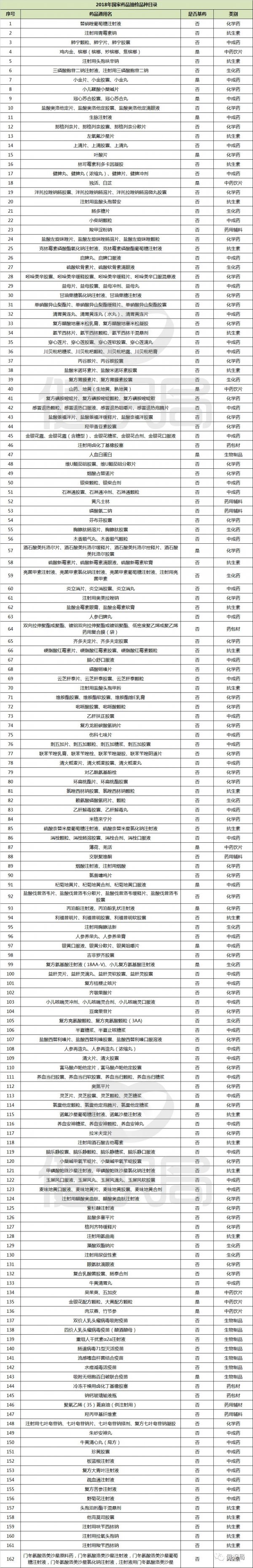
根據《通(tōng)知》顯示,2018年國家藥品抽檢品種共162個(gè),包括化(huà)學藥品49個(gè)、抗生素25個(gè)、生化(huà)藥12個(gè)、中成藥51個(gè)、生物(wù)制品8個(gè)、中藥飲品7組、藥包材4個(gè)、藥用(yòng)輔料6個(gè),其中屬于國家基本藥物(wù)品種19個(gè)。(‘162個(gè)檢查品種’詳見文後附表)
此次藥品抽檢,将根據部分(fēn)品種存在的(de)共性風險和(hé)問題,共設立中藥注射以及熱(rè)原專項、中成藥原粉投料專項、中成藥非法顔色添加專項、中藥飲片專項、滴眼劑專項、抗生素有關物(wù)質和(hé)聚合物(wù)質問題專項、生化(huà)藥專項、活菌制劑專項、門冬氨酸洛美(měi)沙星專項、疫苗專項、藥包材和(hé)藥用(yòng)輔料專項等11個(gè)問題專項檢查。
此外,對(duì)其他(tā)抽檢品種,各承檢機構應按照(zhào)各種存在的(de)風險點不同,逐一開展有針對(duì)性的(de)檢驗、探索性研究和(hé)質量分(fēn)析工作。
《通(tōng)知》指出,各省市食品藥品監管部門應根據國家藥品抽檢工作要求,制定相應的(de)抽樣人(rén)員(yuán)培訓計劃,開展有效的(de)培訓工作,總局将以抽檢方式對(duì)有關單位工作執行情況開展檢查。
抽樣時(shí),應按要求分(fēn)别從藥品生産、經營和(hé)使用(yòng)環節進行樣品抽取,被抽樣單位應有一定覆蓋率和(hé)代表性。對(duì)于在生産環節抽樣的(de)品種(包括進口分(fēn)包裝藥品),應盡量選取藥品經營、使用(yòng)單位進行抽樣。
抽樣工作應于2018年5月(yuè)31日前完成,并按要求報送抽樣工作總結。
《通(tōng)知》指出,各承接機構應根據抽檢計劃安排,按照(zhào)國家藥品标準對(duì)所承建的(de)品種進行全國項目檢驗或部分(fēn)項目檢驗,及時(shí)出具檢驗報告書(shū)。對(duì)抽檢計劃中的(de)膠囊劑品種,還(hái)應對(duì)有摻雜(zá)、摻假嫌疑的(de)藥品,應依據已有的(de)補充檢驗方法進行檢驗,或依法報批補充檢驗方法,并出具檢驗報告書(shū)。
全部檢驗工作應于2018年7月(yuè)31日前完成,并按要求報送檢驗結果及工作總結。
不合格藥品的(de)檢驗結果必須立即通(tōng)過“國家藥品抽檢系統”上報,對(duì)檢驗和(hé)探索性研究中發現的(de)藥品質量風險或安全隐患,需按照(zhào)《食品藥品監管總局辦公廳關于進一步加強國家藥品抽檢管理(lǐ)工作的(de)通(tōng)知》要求,立即将有關情況單獨行文報送總局藥化(huà)監管司,對(duì)檢驗過程中發現的(de)違法違規線索,相關單位和(hé)個(gè)人(rén)不得(de)以任何形式向有關企業、單位、個(gè)人(rén)洩露或通(tōng)報。
附上《2018年國家藥品抽檢計劃的(de)通(tōng)知》全文





162個(gè)檢查品種